В ходе ПЦР-реакции часто встречаются некоторые мешающие факторы.
Ввиду очень высокой чувствительности ПЦР, загрязнение считается одним из наиболее важных факторов, влияющих на результаты ПЦР и способных приводить к ложноположительным результатам.
Не менее важны различные факторы, приводящие к ложноотрицательным результатам. Если один или несколько важных компонентов ПЦР-смеси или самой реакции амплификации ингибируются или подвергаются воздействию, это может затруднить диагностический анализ. Это может привести к снижению эффективности и даже к ложноотрицательным результатам.
Помимо ингибирования, потеря целостности целевой нуклеиновой кислоты может произойти из-за условий транспортировки и/или хранения до подготовки образца. В частности, высокие температуры или ненадлежащее хранение могут привести к повреждению клеток и нуклеиновых кислот. Фиксация клеток и тканей, а также заливка в парафин являются хорошо известными причинами фрагментации ДНК и постоянной проблемой (см. рисунки 1 и 2). В этих случаях даже оптимальная изоляция и очистка не помогут.
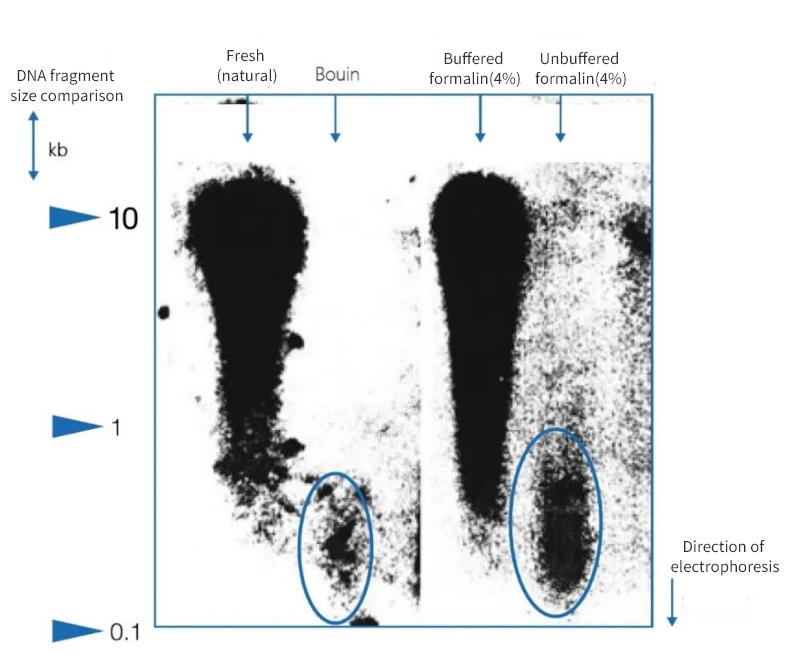
Рисунок 1 | Влияние иммобилизации на целостность ДНК
Электрофорез в агарозном геле показал, что качество ДНК, выделенной из парафиновых срезов аутопсий, значительно варьировалось. В экстрактах присутствовала ДНК различной средней длины фрагментов в зависимости от метода фиксации. ДНК сохранялась только при фиксации в нативных замороженных образцах и в буферном нейтральном формалине. Использование сильнокислого фиксатора Буэна или небуферного формалина, содержащего муравьиную кислоту, приводило к значительной потере ДНК. Оставшаяся фракция сильно фрагментирована.
Слева длина фрагментов выражена в килобазах (кбп).
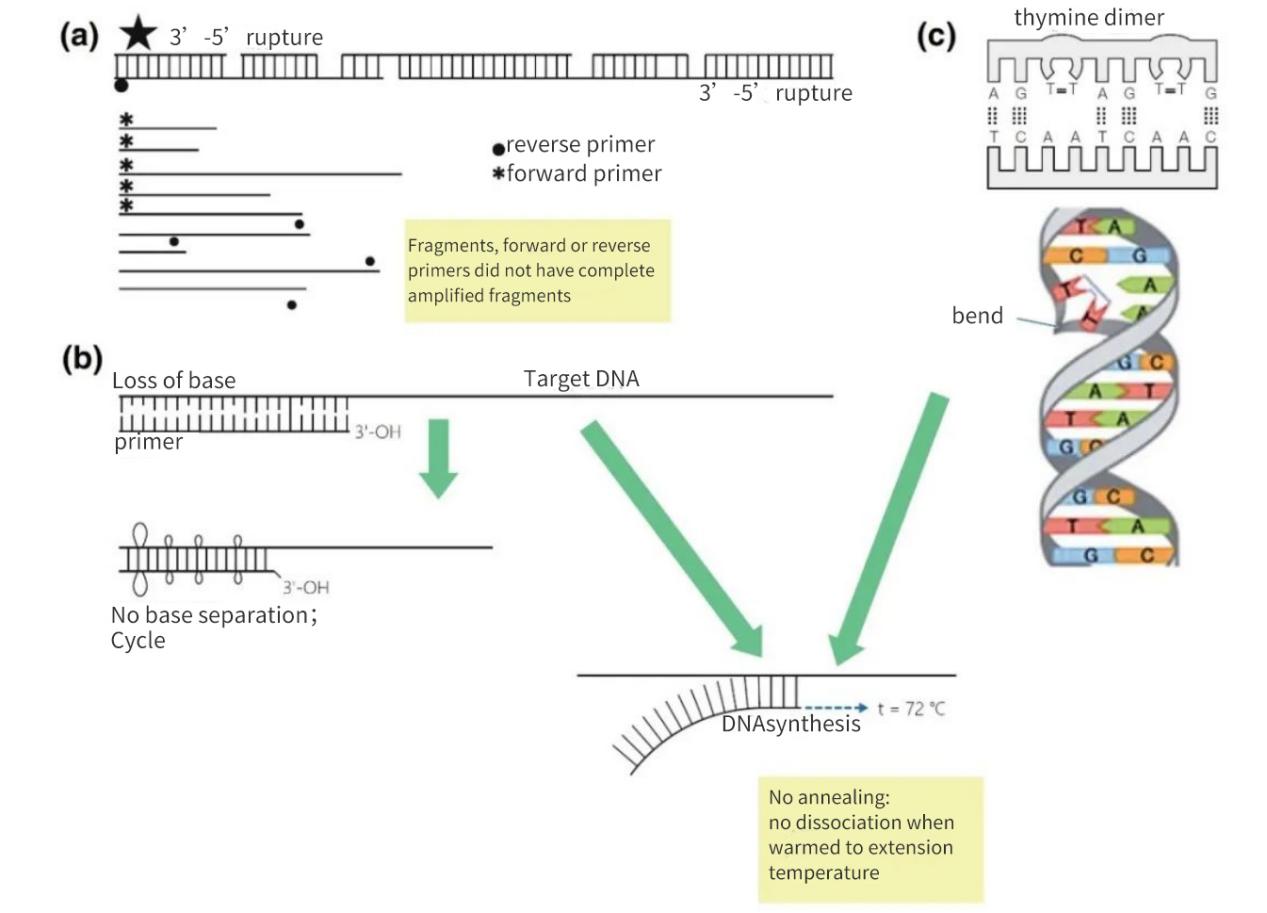
Рисунок 2 | Потеря целостности мишеней нуклеиновых кислот
(а) Разрыв в 3′-5′ нитях на обеих нитях приведет к разрыву целевой ДНК. Синтез ДНК все равно будет происходить на небольшом фрагменте. Однако, если на фрагменте ДНК отсутствует сайт связывания праймера, происходит только линейная амплификация. В наиболее благоприятном случае фрагменты могут повторно насыщать друг друга, но выход будет небольшим и ниже уровня обнаружения.
(b) Потеря оснований, главным образом из-за депуринации и образования димеров тимидина, приводит к уменьшению числа водородных связей и снижению температуры плавления (Tm). В течение длительной фазы нагревания праймеры будут отслаиваться от матричной ДНК и не будут отжигаться даже в менее жестких условиях.
(c) Соседние основания тимина образуют димер ТТ.
Еще одна распространенная проблема, часто встречающаяся в молекулярной диагностике, — это недостаточно эффективное высвобождение целевых нуклеиновых кислот по сравнению с экстракцией фенолом-хлороформом. В крайних случаях это может быть связано с ложноотрицательными результатами. Значительную экономию времени можно получить путем лизиса клеток кипячением или ферментативного расщепления клеточного мусора, но этот метод часто приводит к низкой чувствительности ПЦР из-за недостаточного высвобождения нуклеиновых кислот.
Ингибирование активности полимеразы во время амплификации
В целом, ингибирование используется как обобщающее понятие для описания всех факторов, приводящих к неоптимальным результатам ПЦР. В строго биохимическом смысле ингибирование ограничивается активностью фермента, то есть оно снижает или предотвращает превращение субстрата в продукт посредством взаимодействия с активным центром ДНК-полимеразы или ее кофактором (например, Mg2+ для ДНК-полимеразы Taq).
Компоненты образца или различные буферы и экстракты, содержащие реагенты, могут напрямую ингибировать фермент или связывать его кофакторы (например, ЭДТА), тем самым инактивируя полимеразу и, в свою очередь, приводя к снижению или ложноотрицательным результатам ПЦР.
Однако многие взаимодействия между компонентами реакции и нуклеиновыми кислотами, содержащими целевые молекулы, также обозначаются как «ингибиторы ПЦР». После того, как целостность клетки нарушается в результате изоляции и нуклеиновая кислота высвобождается, могут происходить взаимодействия между образцом и окружающим его раствором и твердой фазой. Например, «поглотители» могут связываться с одно- или двухцепочечной ДНК посредством нековалентных взаимодействий и препятствовать изоляции и очистке, уменьшая количество целевых молекул, которые в конечном итоге достигают реакционного сосуда для ПЦР.
В целом, ингибиторы ПЦР присутствуют в большинстве биологических жидкостей и реагентах, используемых для клинической диагностики (мочевина в моче, гемоглобин и гепарин в крови), пищевых добавках (органические компоненты, гликоген, жиры, ионы Ca2+) и компонентах окружающей среды (фенолы, тяжелые металлы).
| Ингибиторы | Источник |
| Ионы кальция | Молоко, костная ткань |
| Коллаген | Салфетка |
| Желчные соли | Фекалии |
| Гемоглобин | В крови |
| Гемоглобин | образцы крови |
| Гуминовая кислота | Почва, растение |
| Кровь | Кровь |
| Лактоферрин | Кровь |
| (Европейский) меланин | Кожа, волосы |
| Миоглобин | Мышечная ткань |
| Полисахариды | Растение, фекалии |
| Протеаза | Молоко |
| Мочевина | Моча |
| Мукополисахарид | Хрящи, слизистые оболочки |
| Лигнин, целлюлоза | Растения |
Наиболее распространенные ингибиторы ПЦР можно обнаружить в бактериях и эукариотических клетках, нецелевой ДНК, ДНК-связывающих макромолекулах тканевых матриц и лабораторном оборудовании, таком как перчатки и пластмассы. Очистка нуклеиновых кислот во время или после экстракции является предпочтительным методом удаления ингибиторов ПЦР.
Сегодня различное автоматизированное оборудование для экстракции может заменить многие ручные протоколы, но 100% извлечение и/или очистка целевых последовательностей так и не были достигнуты. Потенциальные ингибиторы могут все еще присутствовать в очищенных нуклеиновых кислотах или уже проявить свое действие. Существуют различные стратегии для снижения воздействия ингибиторов. Выбор подходящей полимеразы может существенно повлиять на активность ингибиторов. Другие проверенные методы снижения ингибирования ПЦР включают увеличение концентрации полимеразы или применение добавок, таких как БСА (бычий сывороточный альбумин).
Ингибирование ПЦР-реакций может быть продемонстрировано с помощью внутреннего контроля качества процесса (ВКК).
Необходимо тщательно промыть выделенную нуклеиновую кислоту, удалив из нее все реагенты и другие растворы из набора для экстракции, такие как этанол, ЭДТА, ЦЕТАБ, LiCl, GuSCN, SDS, изопропанол и фенол. В зависимости от их концентрации они могут активировать или ингибировать ПЦР.
Дата публикации: 19 мая 2023 г.
 中文网站
中文网站