Nat Med | Мультиомиксный подход к картированию интегрированного ландшафта опухоли, иммунной системы и микробиоты при колоректальном раке выявляет взаимодействие микробиома с иммунной системой.
Несмотря на то, что биомаркеры первичного рака толстой кишки в последние годы extensively изучались, существующие клинические рекомендации основываются только на стадировании опухоли, лимфатических узлов и метастазов, а также на выявлении дефектов репарации ДНК (MMR) или микросателлитной нестабильности (MSI) (в дополнение к стандартным патологическим исследованиям) для определения рекомендаций по лечению. Исследователи отметили отсутствие связи между иммунными ответами, основанными на экспрессии генов, микробными профилями и стромой опухоли в когорте пациентов с колоректальным раком из Атласа генома рака (TCGA) и выживаемостью пациентов.
По мере развития исследований было установлено, что количественные характеристики первичного колоректального рака, включая клеточную, иммунную, стромальную или микробную природу опухоли, значительно коррелируют с клиническими исходами, однако понимание того, как их взаимодействие влияет на результаты лечения пациентов, по-прежнему ограничено.
Для анализа взаимосвязи между фенотипической сложностью и исходом заболевания группа исследователей из Института медицинских исследований Сидра в Катаре недавно разработала и валидировала интегрированный показатель (mICRoScore), который определяет группу пациентов с хорошими показателями выживаемости путем объединения характеристик микробиома и констант иммунного отторжения (ICR). Группа провела всесторонний геномный анализ свежезамороженных образцов от 348 пациентов с первичным колоректальным раком, включая секвенирование РНК опухолей и соответствующих здоровых тканей толстой кишки, полногеномное секвенирование, глубокое секвенирование генов Т-клеточного рецептора и 16S бактериальной рРНК, дополненное полногеномным секвенированием опухоли для дальнейшей характеристики микробиома. Исследование было опубликовано в журнале Nature Medicine под названием «Интегрированный атлас опухоли, иммунной системы и микробиома при раке толстой кишки».

Статья опубликована в журнале Nature Medicine.
Обзор AC-ICAM
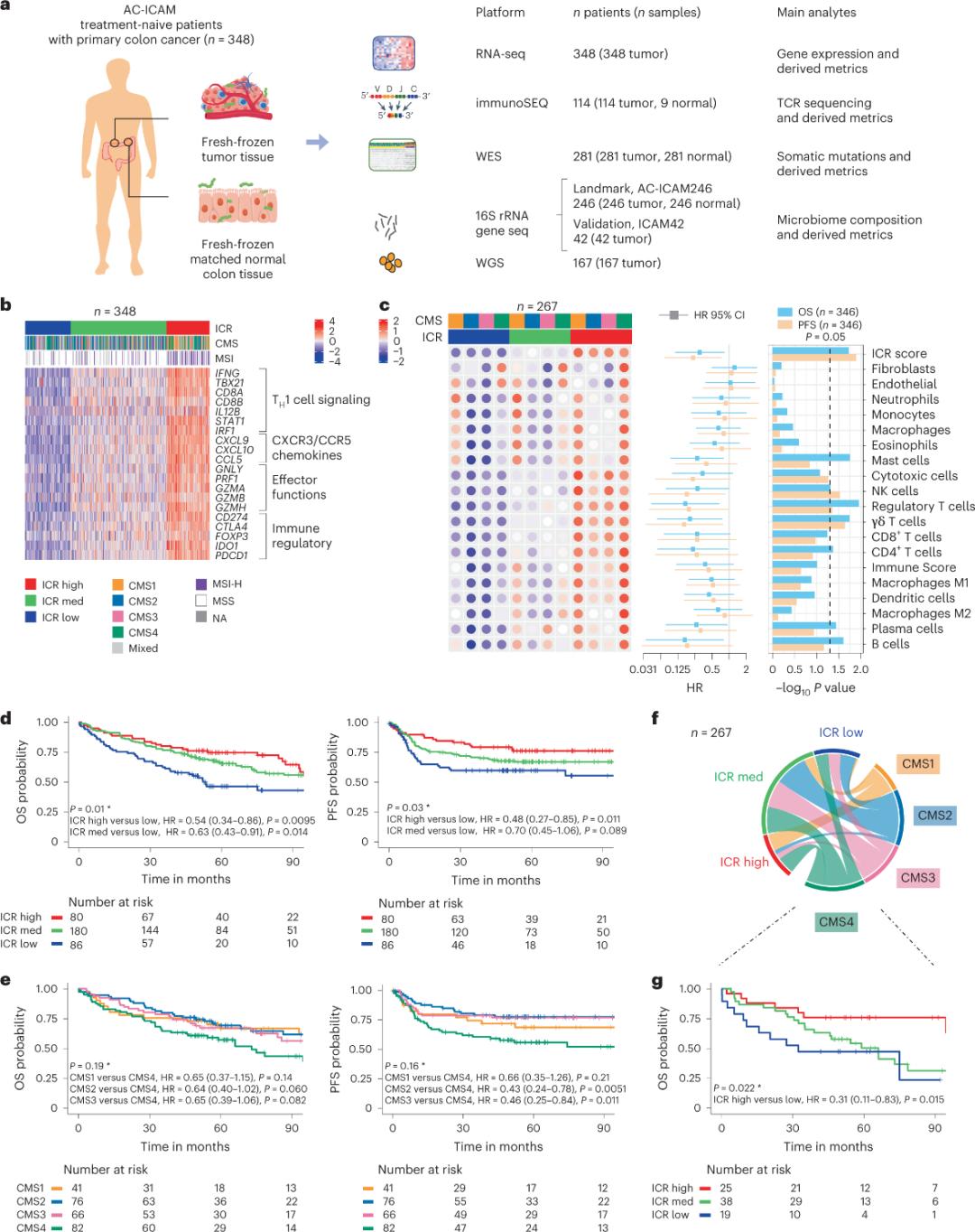
Исследователи использовали ортогональную геномную платформу для анализа свежезамороженных образцов опухолей и соответствующих им образцов здоровой ткани толстой кишки (пары опухоль-норма) от пациентов с гистологически подтвержденным диагнозом рака толстой кишки, не получавших системной терапии. На основе полногеномного секвенирования (WES), контроля качества данных РНК-секвенирования и проверки критериев включения были отобраны геномные данные от 348 пациентов, которые были использованы для дальнейшего анализа со средним периодом наблюдения 4,6 года. Исследовательская группа назвала этот ресурс Sidra-LUMC AC-ICAM: Карта и руководство по взаимодействиям иммунной системы, рака и микробиома (Рисунок 1).
Молекулярная классификация с использованием ICR
Используя модульный набор иммунологических генетических маркеров для непрерывного иммунологического надзора за раком, называемый иммунологической константой отторжения (ICR), исследовательская группа оптимизировала ICR, объединив его в панель из 20 генов, охватывающую различные типы рака, включая меланому, рак мочевого пузыря и рак молочной железы. ICR также ассоциируется с ответом на иммунотерапию при различных типах рака, включая рак молочной железы.
Сначала исследователи подтвердили сигнатуру ICR когорты AC-ICAM, используя подход совместной классификации на основе генов ICR для разделения когорты на три кластера/иммунных подтипа: высокий ICR (горячие опухоли), средний ICR и низкий ICR (холодные опухоли) (Рисунок 1b). Исследователи охарактеризовали иммунную предрасположенность, связанную с консенсусными молекулярными подтипами (CMS), транскриптомной классификацией рака толстой кишки. Категории CMS включали CMS1/иммунный, CMS2/канонический, CMS3/метаболический и CMS4/мезенхимальный. Анализ показал, что показатели ICR отрицательно коррелировали с определенными путями раковых клеток во всех подтипах CMS, а положительные корреляции с иммуносупрессивными и стромальными путями наблюдались только в опухолях CMS4.
Во всех случаях CMS количество естественных клеток-киллеров (NK-клеток) и субпопуляций Т-клеток было самым высоким в иммунных субтипах с высоким уровнем ICR, при этом наблюдалась большая вариабельность в других субпопуляциях лейкоцитов (рис. 1c). Иммунные субтипы ICR имели разные показатели общей выживаемости (OS) и выживаемости без прогрессирования (PFS), с прогрессивным увеличением ICR от низкого к высокому уровню (рис. 1d), что подтверждает прогностическую роль ICR при колоректальном раке.
Рисунок 1. Дизайн исследования AC-ICAM, сигнатура генов, связанных с иммунитетом, иммунные и молекулярные подтипы и выживаемость.
ICR захватывает обогащенные в опухоли, клонально амплифицированные Т-клетки.
Сообщается, что лишь меньшинство Т-клеток, инфильтрирующих опухолевую ткань, специфичны к опухолевым антигенам (менее 10%). Поэтому большинство внутриопухолевых Т-клеток называют «соседними» Т-клетками. Наиболее сильная корреляция с количеством обычных Т-клеток с продуктивными TCR наблюдалась в субпопуляциях стромальных клеток и лейкоцитов (обнаруженных с помощью РНК-секвенирования), которые можно использовать для оценки субпопуляций Т-клеток (рис. 2а). В кластерах ICR (в целом и по классификации CMS) самая высокая клональность иммунных SEQ TCR наблюдалась в группах с высоким уровнем ICR и подтипе CMS1/иммунный (рис. 2с), с наибольшей долей опухолей с высоким уровнем ICR. Используя весь транскриптом (18 270 генов), шесть генов ICR (IFNG, STAT1, IRF1, CCL5, GZMA и CXCL10) вошли в десятку генов, положительно связанных с клональностью TCR по иммунологической последовательности (рис. 2d). Клональность TCR по иммунологической последовательности коррелировала сильнее с большинством генов ICR, чем корреляции, наблюдаемые при использовании опухолечувствительных маркеров CD8+ (рис. 2f и 2g). В заключение, приведенный выше анализ предполагает, что сигнатура ICR отражает наличие обогащенных опухолью, клонально амплифицированных Т-клеток и может объяснить ее прогностическое значение.
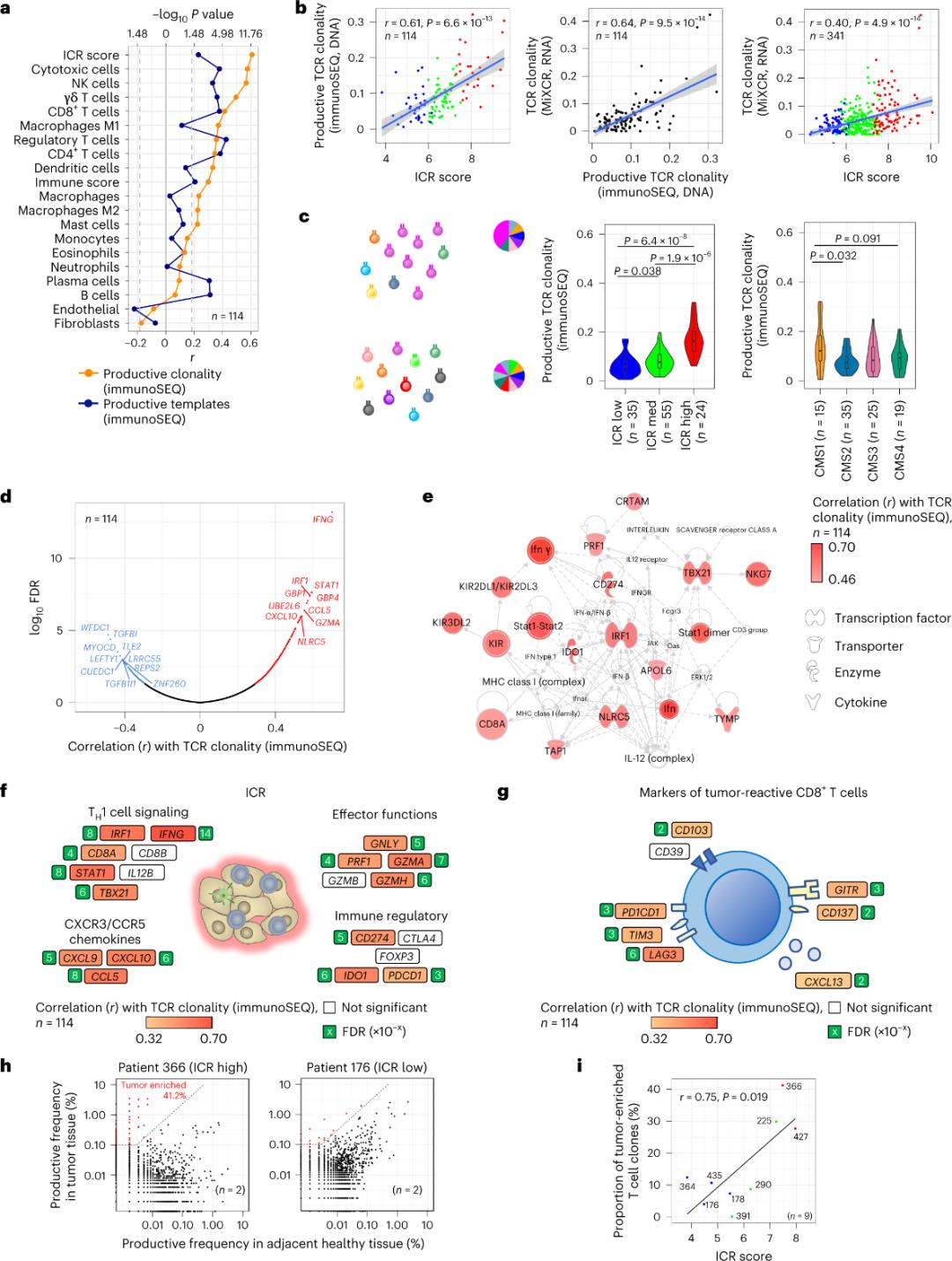
Рисунок 2. Показатели TCR и их корреляция с генами, связанными с иммунитетом, иммунными и молекулярными подтипами.
Состав микробиома в здоровых тканях и тканях, пораженных раком толстой кишки.
Исследователи провели секвенирование 16S рРНК, используя ДНК, выделенную из парных образцов опухолевой и здоровой ткани толстой кишки от 246 пациентов (рис. 3а). Для подтверждения результатов исследователи дополнительно проанализировали данные секвенирования гена 16S рРНК из 42 дополнительных образцов опухолей, для которых не было доступной для анализа нормальной ДНК. Сначала исследователи сравнили относительную численность микрофлоры между парными образцами опухолей и здоровой ткани толстой кишки. Количество Clostridium perfringens было значительно выше в опухолях по сравнению со здоровыми образцами (рис. 3а-3d). Не было обнаружено существенной разницы в альфа-разнообразии (разнообразии и численности видов в одном образце) между образцами опухолей и здоровых образцов, а также наблюдалось умеренное снижение микробного разнообразия в опухолях с высоким ICR по сравнению с опухолями с низким ICR.
Для выявления клинически значимых связей между микробными профилями и клиническими исходами исследователи стремились использовать данные секвенирования гена 16S рРНК для идентификации характеристик микробиома, предсказывающих выживаемость. В рамках проекта AC-ICAM246 исследователи использовали модель регрессии Кокса с учетом общей выживаемости, которая отобрала 41 характеристику с ненулевыми коэффициентами (связанными с дифференциальным риском смертности), называемые классификаторами MBR (рисунок 3f).
В этой обучающей выборке (ICAM246) низкий показатель MBR (MBR<0, низкий MBR) был связан со значительно более низким риском смерти (85%). Исследователи подтвердили связь между низким MBR (риском) и увеличенной общей выживаемостью в двух независимо проверенных выборках (ICAM42 и TCGA-COAD). (Рисунок 3) Исследование показало сильную корреляцию между эндогастральными кокками и показателями MBR, которые были схожи в опухолевой и здоровой ткани толстой кишки.
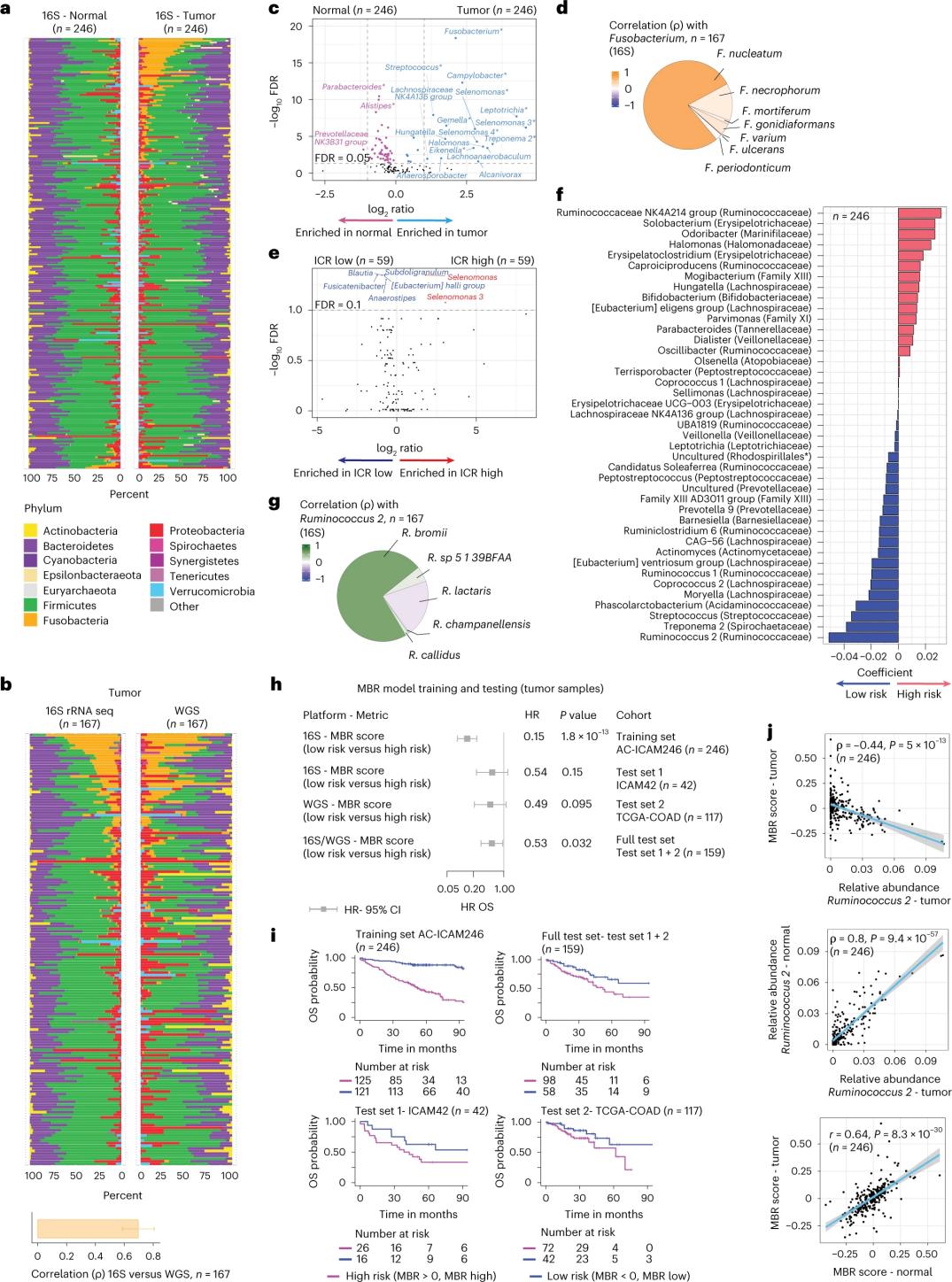
Рисунок 3. Микробиом в опухолевых и здоровых тканях и его связь с ICR и выживаемостью пациентов.
Заключение
Использованный в этом исследовании мультиомиксный подход позволяет тщательно выявлять и анализировать молекулярную сигнатуру иммунного ответа при колоректальном раке и раскрывать взаимодействие между микробиомом и иммунной системой. Глубокое секвенирование TCR опухолевых и здоровых тканей показало, что прогностический эффект ICR может быть обусловлен его способностью выявлять обогащенные в опухоли и, возможно, специфичные для опухолевых антигенов клоны Т-клеток.
Анализируя состав микробиома опухоли с помощью секвенирования гена 16S рРНК в образцах AC-ICAM, команда выявила микробиомную сигнатуру (оценка риска MBR) с высокой прогностической ценностью. Хотя эта сигнатура была получена из образцов опухоли, наблюдалась сильная корреляция между показателями риска MBR здоровой толстой кишки и опухоли, что позволяет предположить, что эта сигнатура может отражать состав кишечного микробиома пациентов. Комбинируя оценки ICR и MBR, удалось идентифицировать и подтвердить мультиомический биомаркер, прогнозирующий выживаемость пациентов с раком толстой кишки. Мультиомический набор данных, полученный в ходе исследования, предоставляет ресурс для лучшего понимания биологии рака толстой кишки и помогает в разработке персонализированных терапевтических подходов.
Дата публикации: 15 июня 2023 г.
 中文网站
中文网站